Transfusionsmedizinische Forschung
Projektbereich 1: Optimierungsstrategien bei der Herstellung von Thrombozytenkonzentraten
Molekulare Mechanismen der „platelet storage lesion“ und Optimierung der Lagerungsbedingungen von Thrombozyten-Konzentraten
Thrombozyten-Konzentrate werden bei einem Mangel oder einer Funktionsstörung von Blutplättchen zur Prophylaxe oder zur Therapie von Blutungen eingesetzt. Gespendete Thrombozyten können bis zu vier Tage gelagert werden. Allerdings büßen sie dabei einen Teil ihrer blutstillenden Eigenschaften ein. Wir versuchen, die molekularen Grundlagen dieser Veränderungen zu entschlüsseln, mit dem Ziel, die Lagerungsbedingungen noch weiter optimieren zu können.
Die Transfusion von Thrombozyten-Konzentraten wird zur Prophylaxe oder zur Therapie von Blutungen bei Thrombozytopenien oder bei Thrombozytenfunktionsstörungen eingesetzt.
Insbesondere Patientinnen und Patienten mit bösartigen Erkrankungen sind im Verlauf der Behandlung, zum Beispiel nach Chemo- oder Radiotherapie, häufig auf die Gabe von Fremd-Thrombozyten angewiesen. Für diesen Zweck werden Thrombozyten von Blutspenderinnen und Blutspendern gewonnen und als Thrombozyten-Konzentrate für bis zu vier Tage gelagert.
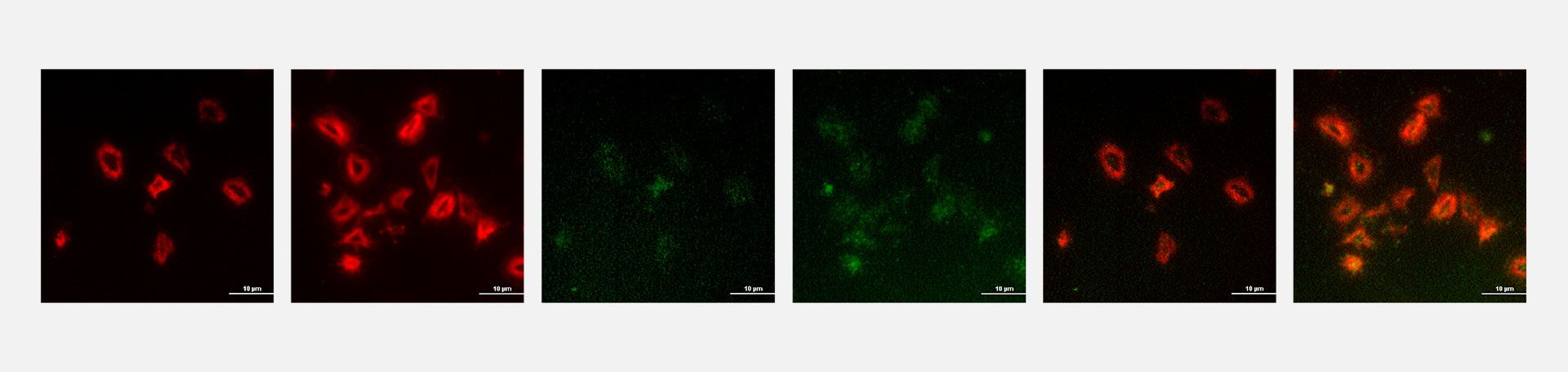
Während der Lagerung treten unter anderem morphologische Veränderungen auf. Die Rezeptorendichte und -zusammensetzung auf der Thrombozytenoberfläche ändert sich. Die gelagerten Thrombozyten weisen eine abnehmende Aktivierbarkeit und Aggregierbarkeit auf und büßen damit einen Teil ihrer hämostatischen Kapazität ein. Dieser Prozess wird als „platelet storage lesion“ bezeichnet. Mit der Abnahme der Thrombozytenfunktion während der Lagerung ist eine geringere Effektivität der transfundierten Thrombozyten verbunden.
Unser Forschungsteam beschäftigt sich damit, welche Veränderungen in den thrombozytären Signaltransduktionswegen in Abhängigkeit von verschiedenen physikalischen und biochemischen Lagerungsbedingungen in Gang gesetzt werden. Im Fokus unserer Forschung steht insbesondere der Einfluss der Lagerungstemperatur auf die funktionellen Eigenschaften der gelagerten Thrombozyten.
Ziel ist es dabei, die Mechanismen aufzuklären, die auf molekularer Ebene zur „platelet storage lesion“ führen. Das Verständnis für diese Prozesse ist eine wesentliche Voraussetzung, um geeignete Strategien für eine Optimierung der Lagerungsbedingungen zu entwickeln.
Das Forschungsvorhaben wird durch die „Stiftung Transfusionsmedizin und Immunhämatologie" der Deutschen Gesellschaft für Transfusionsmedizin und Immunhämatologie (DGTI) gefördert.
Projektbereich 2: Nicht-hämostatische und immunologische Funktionen von Thrombozyten
Die Bedeutung der Toll-like-Rezeptoren und des Proteasom-Systems in humanen Thrombozyten
Wir erforschen die Bedeutung von nicht-hämostatischen Systemen in Thrombozyten. Hierzu gehören die Toll-like-Rezeptoren, die sich auf der Oberfläche von Thrombozyten befinden und die für das Erkennen von Krankheitserregern wichtig sind. Ein weiteres System ist das Proteasom-System, das in kernhaltigen Zellen den Proteinabbau steuert. Es ist bislang wenig darüber bekannt, welche Rolle diese Systeme in Blutplättchen zum Beispiel bei Infektionen, Autoimmunerkrankungen oder Transfusionsreaktionen spielen.
Toll-like-Rezeptoren (TLRs), ansonsten auf Phagozyten und dendritischen Zellen exprimiert, sind für die Erkennung von pathogenen Strukturen bedeutsam und auch auf Thrombozyten nachweisbar. Durch Bindung von bakteriellen Peptiden oder Lipopolysacchariden (LPS) an TLRs können Thrombozyten aktiviert und auf diese Weise weitere Immunantworten ausgelöst werden. Deshalb untersucht unsere Arbeitsgruppe, wie die Funktion der beiden wichtigsten TLRs in Thrombozyten, TLR2 und TLR4, reguliert wird. Zudem ist es für die Transfusion von Bedeutung, wie sich die Funktion der Toll-like-Rezeptoren während der Ex-vivo-Lagerung verändert.
Thrombozyten sind vor allem in Mechanismen der Hämostase und der Thrombusbildung involviert. Als kernlose Zellen sind sie nur zu einer beschränkten De-novo-Proteinsynthese befähigt. Thrombozyten besitzen gleichzeitig aber alle wesentlichen Bestandteile des Proteasomsystems, das die Proteindegradation in eukaryontischen Zellen steuert. Ein weiterer Schwerpunkt unserer Forschungsarbeit ist es deshalb, die physiologische Bedeutung dieses Proteinabbau-Systems in Thrombozyten, insbesondere die Interaktionen mit anderen molekularen und funktionellen Systemen wie den Toll-like-Rezeptorsystemen, aufzuklären.
Das Forschungsvorhaben wird durch die Deutsche Forschungsgemeinschaft (DFG) gefördert (DFG-Projekt KO 5256/4-1, seit 2023).
Auch vorangegangene Projekte wurden von 2018 bis 2021 durch die DFG unterstützt (DFG-Projekte KO 5256/3-1 und KO 5294/2-1).
Kooperation mit wissenschaftlichen Arbeitsgruppen
Das Institut für Klinische Transfusionsmedizin und Hämotherapie arbeitet mit einer Vielzahl von Forschungsgruppen des Universitätsklinikums Würzburg zusammen. Dies geschieht beispielsweise durch die Bereitstellung von Probenmaterial oder durch die Ausführung von notwendigen Laboranalysen im Rahmen von Studien.
Ein weiterer Schwerpunkt liegt in der Gewinnung von Ausgangsstoffen für Prüfarzneimittel, insbesondere von Leukapheresaten für die Herstellung von neu entwickelten CAR-T-Zell-Produkten.
Kontakt, Öffnungszeiten, Sprechzeiten
Blutspende
Bitte vereinbaren Sie telefonisch einen Termin unter
Telefon: +49 931 201-31230
Wichtig
Zum Blutspenden bitte unbedingt Personalausweis oder Reisepass mitbringen!
Telefon
Blutspende
+49 931 201-31230
Immunhämatologisches Labor / Blutbank
+49 931 201-31333
Kommissarischer Direktor
Prof. Dr. med. J. Kößler
+49 931 201-31301
Anschrift
Institut für Klinische Transfusionsmedizin und Hämotherapie des UniversitätsklinikumsWürzburg | Oberdürrbacher Straße 6 | 97080 Würzburg
Blutspende
Zentrum Innere Medizin (ZIM) | Haus A3 | Ebene -3
Blutbank / Immunhämatologisches Labor
Zentrum Operative Medizin (ZOM) | Haus A1 | Ebene -1