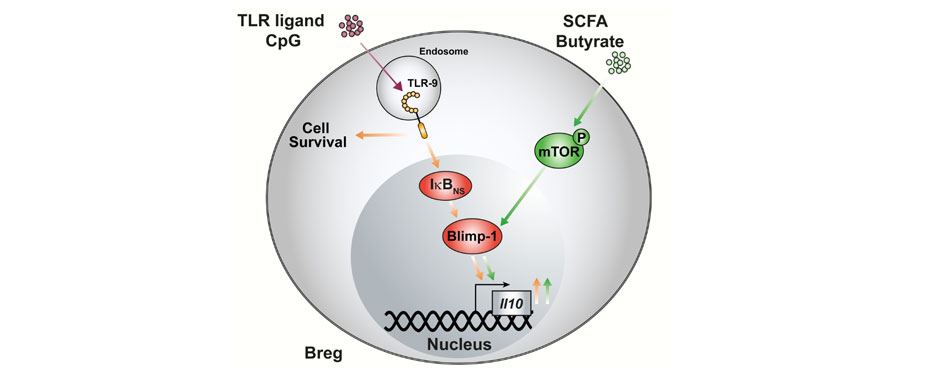
Durch die Kultivierung mit kurzkettigen Fettsäuren der adaptiven Immunzellen, die für die humorale Immunantwort zuständig sind, waren die Forschenden in der Lage, sogenannte regulatorische B-Zellen (Bregs) zu erzeugen, die für die Behandlung von Darmentzündungen im Mausmodell genutzt werden konnten. Die im Journal Mucosal Immunology publizierte Arbeit gibt neue Einsichten in die molekularen Prozesse, die von Metaboliten des Mikrobioms angesprochen und therapeutisch genutzt werden könnten.
Unterstützt wurden die Arbeiten in Würzburg vom Institut für Hygiene und Mikrobiologie, gefördert wurde das Projekt unter anderem im Rahmen der Allianz T2EVOLVE und dem Interdisziplinären Zentrum für Klinische Forschung (IZKF).
Maik Luu, Felix F Krause, Heide Monning, Anne Wempe, Hanna Leister, Lisa Mainieri, Sarah Staudt, Kai Ziegler-Martin, Kira Mangold, Nora Kappelhoff, Yoav D Shaul, Stephan Göttig, Carlos Plaza-Sirvent, Leon N Schulte, Isabelle Bekeredjian-Ding, Ingo Schmitze, Ulrich Steinhoff, Alexander Visekruna. Dissecting the metabolic signaling pathways by which microbial molecules drive the differentiation of regulatory B cells. Mucosal Immunology. September 17, 2024. doi:10.1016/j.mucimm.2024.09.003



