Prof. Dr. Christoph Härtel, Direktor der Kinderklinik und Leiter der klinischen Studie PRIMAL, und sein multizentrisches Team haben jetzt in der renommiertesten pädiatrischen Fachzeitschrift JAMA Pediatrics erste Ergebnisse der Studie zur Wirksamkeit von Probiotika zur Vermeidung einer ungünstigen Darmbesiedlung bei Frühgeborenen veröffentlicht.
PRIMAL ist der Name des Konsortiums, das sich im Rahmen der Förderinitiative des Bundesministeriums für Bildung und Forschung (BMBF) „Gesund - ein Leben lang“ im Jahr 2016 gebildet hat. Die Abkürzung steht für PRiming IMmunity At the beginning of LIFE - Prägung der Immunität am Beginn des Lebens.
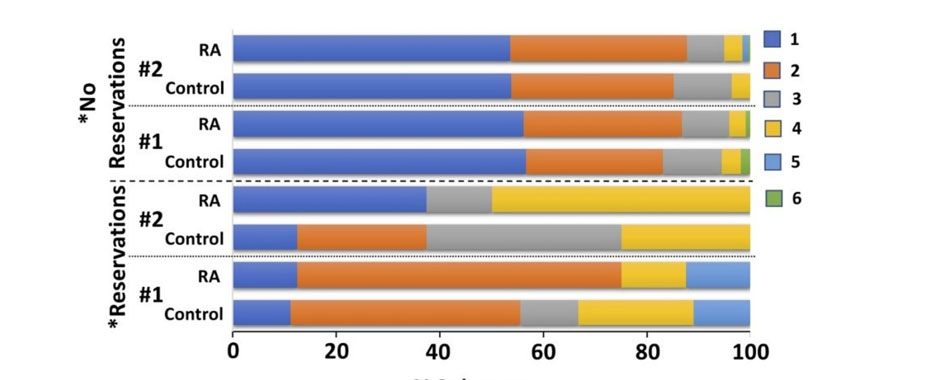
Das Ergebnis der Studie: Bifidobakterien und Laktobazillen konnten die Besiedlung mit multiresistenten Bakterien in den ersten 30 Lebenstagen nicht verhindern, förderten aber die Reifung des Mikrobioms.
Thea Van Rossum, Annette Haiß, Rebecca L. Knoll, Janina Marißen, Daniel Podlesny, Julia Pagel, Marina Bleskina, Maren Vens, Ingmar Fortmann, Bastian Siller, Isabell Ricklefs, Jonas Klopp, Katja Hilbert, Claudius Meyer, Roman Thielemann, Sybelle Goedicke-Fritz, Martin Kuntz, Christian Wieg, Norbert Teig, Thorsten Körner, Angela Kribs, Hannes Hudalla, Markus Knuf, Anja Stein, Christian Gille, Soyhan Bagci, Frank Dohle, Hans Proquitté, Dirk M. Olbertz, Esther Schmidt, Lutz Koch, Sabine Pirr, Jan Rupp, Juliane Spiegler, Matthias V. Kopp, Wolfgang Göpel, Egbert Herting, Sofia K. Forslund, Dorothee Viemann, Michael Zemlin, Peer Bork, Stephan Gehring, Inke R. König, Philipp Henneke, Christoph Härtel. Bifidobacterium and Lactobacillus Probiotics and Gut Dysbiosis in Preterm Infants: The PRIMAL Randomized Clinical Trial. JAMA Pediatr. Published online August 05, 2024. doi:10.1001/jamapediatrics.2024.2626.