Würzburg. PRIMAL ist der Name des Konsortiums, das sich anlässlich der Förderinitiative des Bundesministeriums für Bildung und Forschung (BMBF) „Gesund - ein Leben lang“ im Jahr 2016 gebildet hat. Die Abkürzung steht für PRiming IMmunity At the beginning of LIFE – Prägung der Immunität am Anfang des Lebens. Im Mittelpunkt des deutschlandweiten Netzwerks von Expertinnen und Experten aus der Kinder- und Jugendmedizin und den Naturwissenschaften steht der Darm. Die Zusammensetzung der Darmflora zu Beginn des Lebens ist von entscheidender Bedeutung für die Prägung des Immunsystems und damit für die lebenslange Gesundheit.
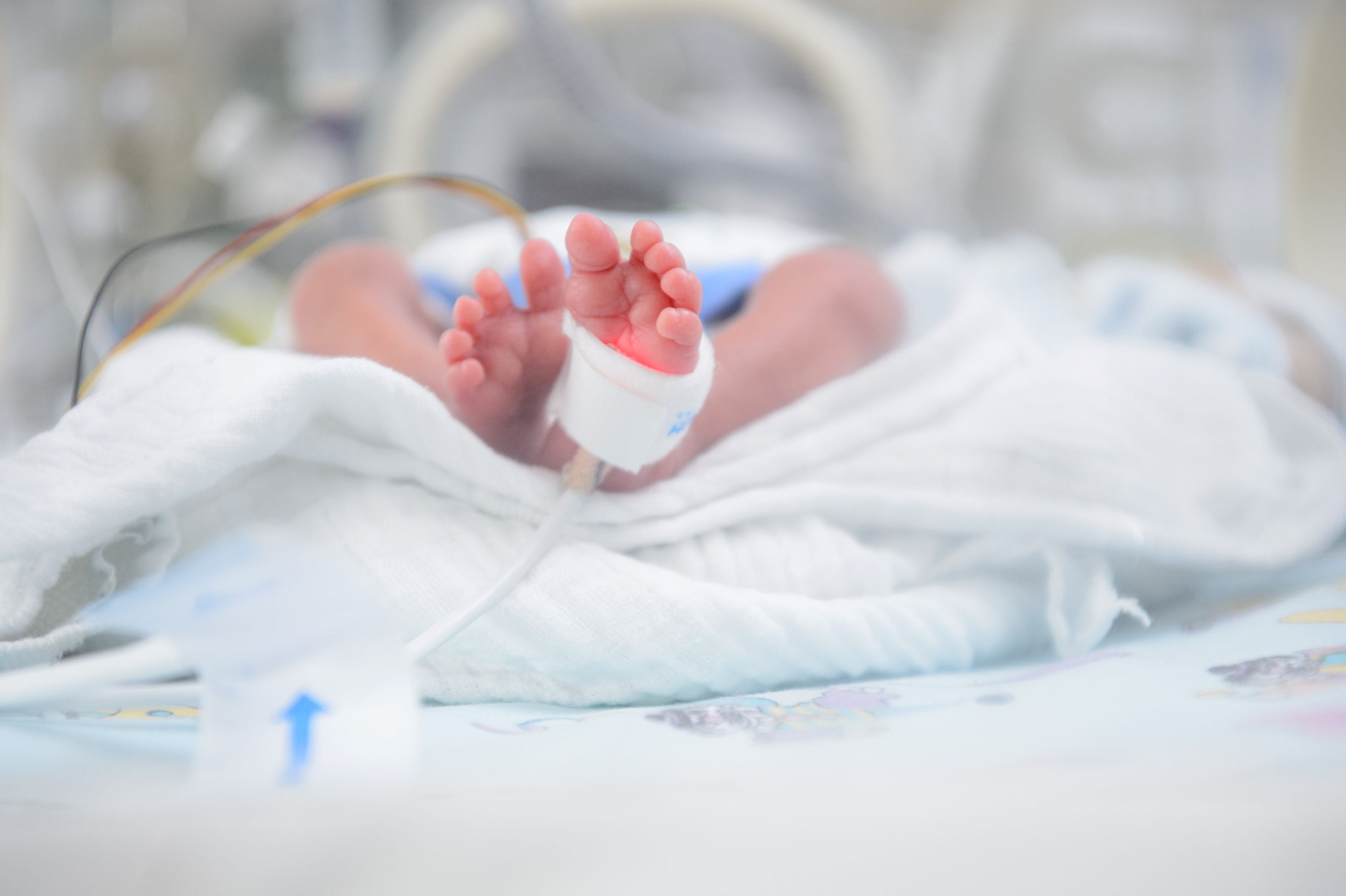
Frühgeborene sind besonders anfällig für Störungen der Darmbesiedlung und damit möglicherweise auch für spätere Erkrankungen wie Asthma, Autoimmunerkrankungen, metabolische Störungen oder Übergewicht. Prof. Dr. Christoph Härtel, Direktor der Kinderklinik des Universitätsklinikums Würzburg (UKW) und Leiter der klinischen PRIMAL-Studie, hat jetzt mit seinem multizentrischen Team in der renommiertesten pädiatrischen Fachzeitschrift JAMA Pediatrics erste Ergebnisse der Untersuchung zur Wirksamkeit von Probiotika zur Vermeidung einer ungünstigen Darmbesiedlung bei Frühgeborenen veröffentlicht.
Gesundes und vielfältiges Mikrobiom unterstützt die Reifung des Immunsystems
„Der Goldstandard für die Entwicklung des Immunsystems ist für uns das reife, gestillte, Antibiotika unbehandelte Neugeborene, das nie vom elterlichen Kontakt getrennt war und bestenfalls mit Geschwistern aufwächst“, erklärt Christoph Härtel, der die Studie in Lübeck begonnen hat, wo er bis 2020 als Spezialist für Neugeborenen- und Intensivmedizin und Leiter des Bereichs Pädiatrische Infektiologie, Immunologie und Rheumatologie am Universitätsklinikum Schleswig-Holstein tätig war. Frühgeborene sind am Anfang des Lebens einer nicht-physiologischen Umwelt ausgesetzt. Somit fehlt ihnen die Möglichkeit, sich so vielfältig zu besiedeln wie reifgeborene Kinder. Durch die Umgebung der Intensivstation und den häufigen Einsatz von Antibiotika bei Frühgeborenen aufgrund deren Infektanfälligkeit wird das Gleichgewicht der Mikroorganismen oft gestört. Es kommt zur Besiedelung mit Antibiotika-resistenten Keimen, welche die Reifung des Immunsystems und die Ausbildung einer effektiven Immunantwort negativ beeinflussen können.
Frühgeborene erhielten 28 Tage lang Bifidobakterien und Lactobazillen
Um dies zu kompensieren, hatte das Konsortium die Idee, den Kindern Probiotika, also lebende Mikroorganismen, in die Muttermilch, Spendermilch oder die künstliche Frühgeborenennahrung, zu geben. Die „Champions“, die natürlicherweise im Mikrobiom reifer, gesunder Neugeborener vorkommen, sind Bifidobakterien und Lactobazillen. In insgesamt 18 Perinatalzentren wurden 643 Kinder, die zwischen der 28. und 33. Schwangerschaftswoche geboren wurden, nach Geschlecht und Gestationsalter gleichverteilt in die randomisierte, placebokontrollierte Doppelblindstudie eingeschlossen. Die Behandlung begann innerhalb der ersten 72 Stunden nach der Geburt und dauerte 28 Tage. Am 30. Lebenstag wurde das Mikrobiom der jungen Studienteilnehmenden untersucht.
Probiotika modulieren Mikrobiom in Richtung Eubiose
Die Probiotika konnten die Besiedlung mit multiresistenten Bakterien nicht verhindern: In beiden Gruppen - Studien- und Kontrollgruppe - waren 37 Prozent der Kinder mit sogenannten MDRO+-Bakterien besiedelt (MDRO steht für Multidrug-Resistant Organism). Das Studienteam konnte jedoch beobachten, dass die Kinder, die Probiotika erhalten hatten, eine schnellere Reifung ihres Mikrobioms aufwiesen. Durch die Gabe von Probiotika war ihr Mikrobiom fast so gut ausgereift wie das von Kindern, die termingerecht geboren wurden. In der Fachsprache wird dieses harmonische Gleichgewicht zwischen den verschiedenen Mikroorganismen im Darm als Eubiose bezeichnet. Die schnellere Reifung des Frühgeborenen-Mikrobioms durch Probiotika im ersten Lebensmonat sei schon mal ein hoffnungsvolles Zwischenergebnis, sagt Christoph Härtel.
Erste Studienkinder kommen jetzt in die Schule: Gibt es Zusammenhang mit ADHS?
Jetzt gilt es die Daten nach dem ersten und zweiten Lebensjahr auszuwerten und weitere Langzeituntersuchungen zu planen, um neue Erkenntnisse darüber zu gewinnen, welche Konsequenzen die frühe Probiotikabehandlung für die kindliche Gesundheit hat. Die ersten Kinder, die an der kontrollierten Studie teilgenommen haben, kommen jetzt in die Schule – ein spannendes Alter, das zum Beispiel Aufschluss über einen vermuteten Zusammenhang zwischen gestörter Darmflora und Autismus, ADHS, Asthma und Adipositas geben könnte.
PRIMAL-Konsortium mit mehreren Projekten
Neben der klinischen PRIMAL-Studie gibt es innerhalb des Konsortiums weitere Projekte aus der Grundlagenforschung und der translationalen Pädiatrie zur Erforschung der Immun-Mikrobiom-Interaktion. Prof. Philipp Henneke vom Centrum für Chronische Immundefizienz (CCI) am Universitätsklinikum Freiburg leitet neben der Koordination des PRIMAL-Konsortiums das Projekt Immunmetabolismus. Prof. Stephan Gehring von der Universitätsmedizin Mainz ist zusammen mit Prof. Peer Bork vom European Molecular Biology Laboratory (EMBL) in Heidelberg für das Projekt der Mikrobiomanalyse verantwortlich. Prof. Michael Zemlin vom Universitätsklinikum des Saarlandes beschäftigt sich in PRIMAL mit Impfantworten nach früher Probiotikatherapie. Prof. Christian Gille vom Universitätsklinikum Heidelberg untersucht mit seinem Team die Rolle von myeloischen Suppressorzellen (MDSC) und Granulozyten. Prof. Dorothee Viemann, Leiterin des Bereichs Translationale Pädiatrie am UKW, analysiert in PRIMAL systematisch die Immunzellprofile der Studienteilnehmenden als wesentlichen Beitrag zum besseren Verständnis der frühkindlichen Mikrobiom-Immun-Interaktion. Gemeinsam mit Dorothee Viemann, Henner Morbach und vielen Kooperationspartnerinnen und -partnern aus den benachbarten Kliniken, Institutionen und Grundlagenwissenschaften wie zum Beispiel der Systemimmunologie möchte Christoph Härtel den Würzburger Forschungsschwerpunkt für die Immunentwicklung im Kindesalter weiter ausbauen.
Erforschung des Mikrobioms steckt noch in den Kinderschuhen
Die Erforschung des Mikrobioms und seiner Rolle für die lebenslange Gesundheit hat in den vergangenen Jahren bereits große Fortschritte gemacht und wichtige Erkenntnisse geliefert. In vielen Bereichen steckt sie aber noch in den Kinderschuhen. Es gibt noch immer zahlreiche offene Fragen darüber, wie die verschiedenen Mikroben miteinander und mit dem menschlichen Körper interagieren und wie spezifische Veränderungen im Mikrobiom bestimmte Krankheiten beeinflussen können.
Projektwebseite: https://primal-studie.de/
Publikation: Thea Van Rossum, Annette Haiß, Rebecca L. Knoll, Janina Marißen, Daniel Podlesny, Julia Pagel, Marina Bleskina, Maren Vens, Ingmar Fortmann, Bastian Siller, Isabell Ricklefs, Jonas Klopp, Katja Hilbert, Claudius Meyer, Roman Thielemann, Sybelle Goedicke-Fritz, Martin Kuntz, Christian Wieg, Norbert Teig, Thorsten Körner, Angela Kribs, Hannes Hudalla, Markus Knuf, Anja Stein, Christian Gille, Soyhan Bagci, Frank Dohle, Hans Proquitté, Dirk M. Olbertz, Esther Schmidt, Lutz Koch, Sabine Pirr, Jan Rupp, Juliane Spiegler, Matthias V. Kopp, Wolfgang Göpel, Egbert Herting, Sofia K. Forslund, Dorothee Viemann, Michael Zemlin, Peer Bork, Stephan Gehring, Inke R. König, Philipp Henneke, Christoph Härtel. Bifidobacterium and Lactobacillus Probiotics and Gut Dysbiosis in Preterm Infants: The PRIMAL Randomized Clinical Trial. JAMA Pediatr. Published online August 05, 2024. doi:10.1001/jamapediatrics.2024.2626
Text: Kirstin Linkamp / UKW