Würzburg. Etwa jeder 25. ist vom Fibromyalgie-Syndrom (FMS) betroffen, einer chronischen Erkrankung, die durch Schmerzen in mehreren Körperregionen gekennzeichnet ist. Begleitsymptome sind Erschöpfung, Schlaf- und Konzentrationsstörungen sowie psychische Belastungen. Da FMS „von außen“ nicht sichtbar ist und der Weg zur Diagnose oft langwierig ist, leiden Patientinnen und Patienten neben den Symptomen oft auch darunter, in ihrer Krankheit nicht verstanden oder akzeptiert zu werden.
Objektiv messbare Marker helfen, Stigma abzubauen
„Die Ursachen des FMS liegen noch im Unklaren, was die gesicherte Diagnose und effektive Behandlung erschwert. Es gibt nur wenige biologische, objektiv messbare Marker für FMS“, berichtet Prof. Dr. Nurcan Üçeyler, leitende Oberärztin in der Neurologie des Universitätsklinikums Würzburg (UKW). „Bislang können unsere Therapien symptomatisch und durch Austesten verschiedener multimodaler Ansätze eine Linderung, aber keine Heilung bewirken.“ In ihrer aktuellen Studie in der Fachzeitschrift PAIN zeigen Nurcan Üçeyler und ihr Team jedoch objektiv messbare Marker, die in Zukunft helfen könnten, FMS schneller und besser zu diagnostizieren und damit unter anderem die Stigmatisierung abzubauen. Auf Basis der neuen Erkenntnisse könnten zudem neue innovative Behandlungsansätze entwickelt werden, um die Beschwerden zu lindern und die sozioökonomische Belastung für die Gesellschaft angesichts der hohen Prävalenz und der hohen Krankheitslast zu reduzieren.
RNA-Analyse bei Patientinnen mit FMS im Vergleich zu gesunden Probandinnen und Frauen mit Depression und chronischen Schmerzen
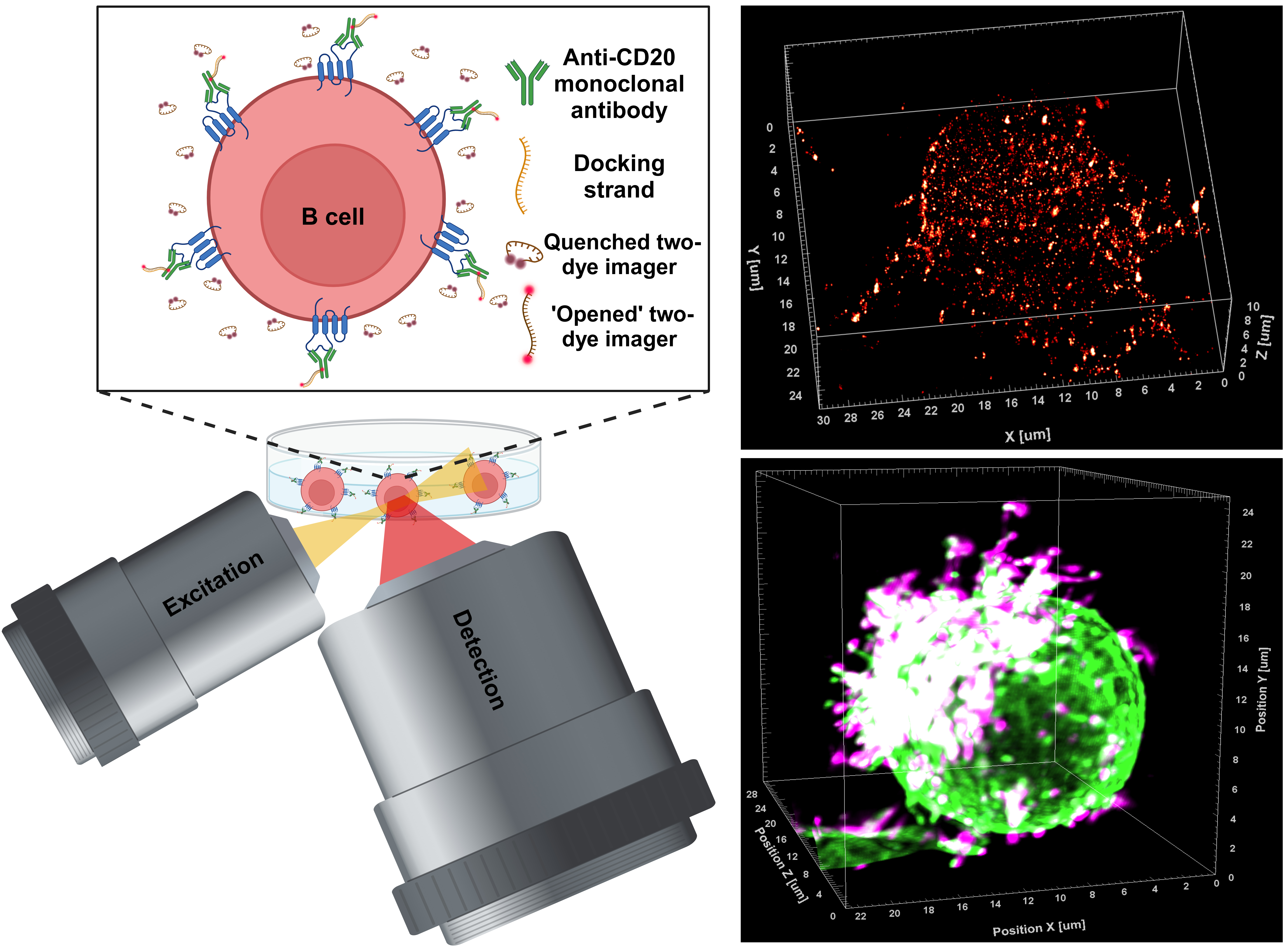
Auf der Suche nach messbaren Veränderungen haben die Forschenden kleine, nicht-kodierende Ribonukleinsäuren (RNAs) aus dem Blut und den Hautzellen von FMS-Patientinnen gewonnen. RNAs sind wichtige Informations- und Funktionsträgerinnen einer Zelle. Konkret wurden RNA-Moleküle wie microRNAs und tRNA-Fragmente untersucht, die bei der Steuerung der Zellaktivität und der Genexpression eine Rolle spielen. „Wir haben diese kleinen RNAs nicht nur mit denen gesunder Frauen verglichen, sondern auch mit denen von Patientinnen mit ähnlichem Krankheitsbild, aber anderer Ätiologie, nämlich Patientinnen mit Depression und chronischen Schmerzen“, erklärt Dr. Christoph Erbacher. Der wissenschaftliche Mitarbeiter in der Neurologie und Erstautor der Studie geht ins Detail: „Mit Hilfe moderner RNA-Sequenzierungstechniken konnten wir zeigen, dass einige kleine RNAs wie hsa-miR-182-5p und hsa-miR-576-5p bei FMS-Patientinnen vermehrt im Blut vorkommen. Bei Patientinnen mit schwerer Depression und chronischen Schmerzen sind sie sogar noch stärker erhöht. Auch in Hautzellen und innerhalb der bisher wenig erforschten Klasse der tRNA-Fragmente konnten wir Unterschiede nachweisen.“
„Mehrere kleine RNAs waren mit der Schwere der Symptome assoziiert“
Die Möglichkeit, unterschiedlich regulierte kleine RNAs im Blut oder in der Haut zu bestimmen, stellt somit eine minimalinvasive Perspektive zur Verbesserung der Diagnose dar. Mehrere kleine RNAs wurden auch mit dem Schweregrad der Symptome in Verbindung gebracht, beispielsweise mit der Ausdehnung des Schmerzes im Körper und der empfundenen Schmerzstärke, was zur Verlaufskontrolle der Krankheit oder zur Einteilung der Patientinnen und Patienten in diagnostische und eventuell auch therapeutische Subgruppen genutzt werden kann. Schließlich haben die kleinen RNAs bekannte und teilweise unbekannte Funktionen in den Körperzellen.
RNAs in Hautzellen stehen im Zusammenhang mit Schmerzreizen, RNAs im Blut sind an der Regulation von Immunzellen beteiligt
Interessant ist laut Erbacher auch die Erkenntnis, dass die beschriebenen Veränderungen von microRNAs und tRNA-Fragmenten in den Hautzellen mit den bereits beschriebenen Nervenschädigungen an den kleinen Nervenfasern der Haut zusammenhängen könnten. Diese Nervenfasern vermitteln die Wahrnehmung potenziell schmerzhafter äußerer Reize. Die im Blut von FMS-Patientinnen gefundenen kleinen RNAs sind dagegen an der Regulation von Immunzellen beteiligt, was in Übereinstimmung mit anderen aktuellen Studien eine Beteiligung des Immunsystems an den Symptomen des FMS nahelegt.
Validierung in einer größeren Kohorte und Studie an Männern
Wann können Betroffene und Behandelnde von den Erkenntnissen profitieren? „Bevor zum Beispiel ein Bluttest etabliert werden kann, müssen die kleinen RNAs in einer neuen, größeren Kohorte validiert werden“, antwortet Nurcan Üçeyler. Außerdem sollen die gefundenen Unterschiede auch in der bisher unterrepräsentierten Gruppe der Männer mit FMS untersucht werden. Zudem gilt es zu prüfen, in welchen Immunzellen im Blut diese Veränderungen auftreten und wie sie zum Beispiel die Ausschüttung von Botenstoffen und Antikörpern modulieren.
Dank an Kooperationspartner, Förderer sowie Patientinnen und Probandinnen
Die Studie wurde interdisziplinär gemeinsam mit Grundlagenwissenschaftlerinnen und -wissenschaftlern der Hebrew University of Jerusalem (HUJI) und intersektoral mit ärztlichen Kolleginnen und Kollegen der Klinik für Psychiatrie, Psychosomatik und Psychotherapie des UKW durchgeführt.
Das Projekt wurde finanziell unterstützt von der Deutschen Forschungsgemeinschaft (DFG) und der Israel Science Foundation, Keter Holdings und der Ken Stein Familienstiftung. Ein besonderer Dank gilt den zahlreichen Patientinnen und gesunden Probanden, durch deren Teilnahme die der Studie zugrundeliegenden Untersuchungen erst möglich wurden.
Publikation:
Erbacher C, Vaknine-Treidel S, Madrer N, Weinbender S, Evdokimov D, Unterecker S, Moshitzky G, Sommer C, Greenberg DS, Soreq H, Üçeyler N. Altered blood and keratinocyte microRNA/transfer RNA fragment profiles related to fibromyalgia syndrome and its severity. Pain. 2024 Dec 6. doi: 10.1097/j.pain.0000000000003499. Epub ahead of print. PMID: 39679614.