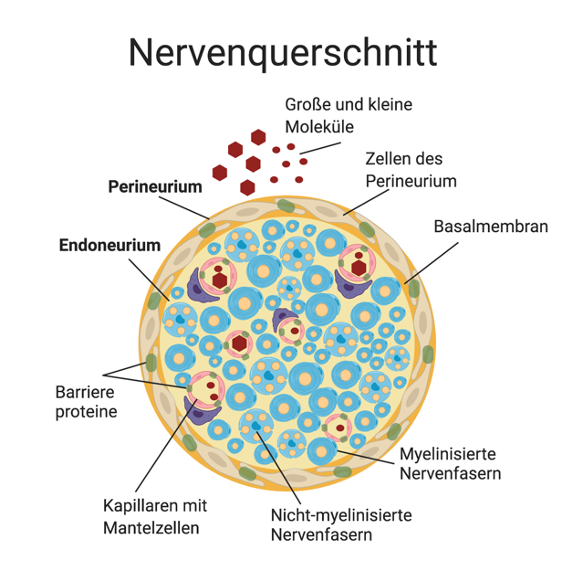
Blut-Nerven-Schranke
Der periphere Nerv, der für die elektrische Weiterleitung von Signalen wie etwa des Körperempfindens oder der Bewegung verantwortlich ist, wird über die Blut-Nerven-Schranke gegen schädigende äußere Einflüsse besonders geschützt. So eine Blut-Nerven-Barriere besteht aus zwei Zellschichten, der Zellhülle und der Basalmembran, sowie den Kapillaren innerhalb des Nervs. Wird diese Schranke geschädigt, wird sie durchlässig und hebt den selektiven Stoffdurchtritt auf. Das hat auch negative Auswirkungen auf die elektrische Weiterleitung der Nervensignale.
Forschungsziel
Das Projekt 7 untersucht die Wiederherstellung der Blut-Nerven-Barriere auf zellulärer und molekularer Ebene, parallel zur Schmerzrückbildung nach Nervenschäden unter Einfluss von körpereigenem Netrin. Netrin ist ein Wachstumsfaktor, der die Wachstumsrichtung von Nervenzellen in der Embryonalentwicklung steuert. Neuere Ergebnisse weisen darauf hin, dass Netrin nach Abschluss der Reifung des Nervensystems auch die Blut-Nerven-Barriere im Körper stabilisiert.
Vorgehensweise
Dazu nutzen wir präklinische Modelle der Nervenschädigung, anhand derer wir die Einwirkung und Funktion von Netrin beobachten. Als präklinische Modelle werden zum einen die chronische Nervenligatur, bei der der Nerv abgeschnürt wird, zum anderen die durch das Chemotherapeutikum Bortezomib ausgelöste Polyneuropathie verwendet. Diese Krankheitsmodelle stellt das Projekt 7 auch anderen Projektgruppen der KFO 5001 zur Verfügung.
Im translationalen Teil des Projekts analysieren wir Hautproben mit den Ausläufern der Nerven sowie die Seren von Patientinnen und Patienten mit komplexem regionalem Schmerzsyndrom und Neurofibromatose auf Schrankenproteine und Netrine.
Moderne Techniken
In Haut- und Gewebeproben etablieren wir hochauflösende mikroskopische Verfahren zur Messung der Barrierefunktion für unterschiedliche Molekülgrößen. In Kooperation mit dem Institut für klinische Physiologie der Charité Berlin lassen sich durch spezielle Techniken in vitro Modelle für eine detaillierte Charakterisierung der Nervenbarrieren erstellen, elektrophysiologische Eigenschaften analysieren, der Moleküldurchtritt messen und die Tight Junction-Proteinexpression – Veränderungen in den Barrieremolekülen – quantifizieren. Darüber hinaus ist auch ein Resolutionsmodell der Barriere geplant, das die molekularen Veränderungen der Blut-Nerven-Schranke bei Barriereversiegelung darstellt, die parallel zur Schmerzauflösung auftritt.
Bedeutung für Patientinnen und Patienten
In anderen medizinischen Fachrichtungen werden bereits Medikamente untersucht, die Wachstumsfaktoren unterstützen. Möglicherweise könnten auch Netrine als Wirkstoffe zur Behandlung von Nervenschmerzen genutzt werden, indem sie durch Barriereversiegelung die Schmerzauflösung fördern.
Forschungsteam P7
Leitung
PD Dr. rer. nat. Susanne Krug
Arbeitsgruppen-Leiterin Abteilung Physiologie und Ernährungsmedizin
Charité – Universitätsmedizin Berlin,
Campus Benjamin Franklin
Univ.-Prof. Dr. med. Heike Rittner
Wissenschaftliche Leitung von KFO 5001
Leiterin des Schmerzzentrums des Universitätsklinikums Würzburg
Mitarbeiter im Team
Lukas Knobe, Charité – Universitätsmedizin Berlin
Liste ausgewählter Publikationen
Reinhold AK, Yang S, Chen JT, Hu L, Sauer RS, Krug SM, Mambretti EM, Fromm M, Brack A, Rittner HL (2019)
Tissue plasminogen activator and neuropathy open the blood-nerve barrier with upregulation of microRNA-155-5p in male rats
Biochim Biophys Acta Mol Basis Dis. 2019 Jun 1; 1865(6):1160-1169.
Zur Publikation
Krug SM, Fromm M (2020)
Special Issue on "The Tight Junction and Its Proteins: More than Just a Barrier"
Int J Mol Sci. 2020 Jun 29;21(13):4612.
Zur Publikation
Krug SM, Amasheh M, Dittmann I, Christoffel I, Fromm M, Amasheh S (2013)
Sodium caprate as an enhancer of macromolecule permeation across tricellular tight junctions of intestinal cells
Biomaterials 2013 Jan;34(1):275-82.
Zur Publikation
Hackel D, Krug SM, Sauer RS, Mousa SA, Böcker A, Pflücke D, Wrede EJ, Kistner K, Hoffmann T, Niedermirtl B, Sommer C, Bloch L, Huber O, Blasig IE, Amasheh S, Reeh PW, Fromm M, Brack A, Rittner HL (2012)
Transient opening of the perineurial barrier for analgesic drug delivery
Proc Natl Acad Sci U S A. 2012 Jul 17; 109 (29):E2018-27.
Zur Publikation
Kontakt
Univ.-Prof. Dr. med.
Heike Rittner
Leiterin der Projekte Adhäsions-GPCR CIRL (P6) und Netrin (P7)
+49 931 201-30251