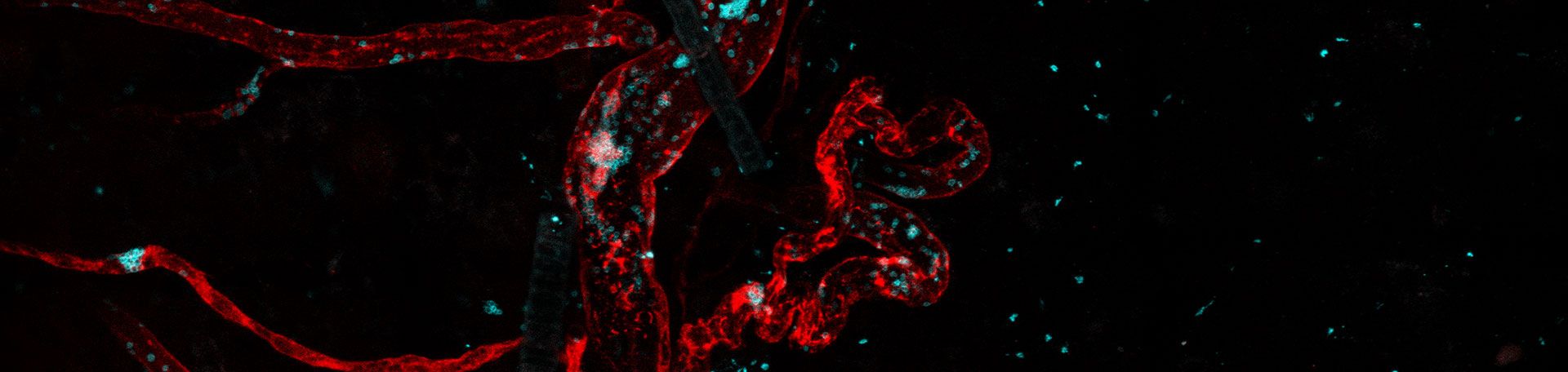
Die Rolle der Thrombozyten bei Tumorwachstum und der Bildung von Metastasen
Krebserkrankungen gehören weltweit zu den häufigsten Ursachen für Morbidität und Mortalität. Frühe Studien zur Charakterisierung von Veränderungen, die Onkogene und Tumorsuppressoren betreffen, trugen dazu bei, die Grundlagen der Krebsbiologie zu etablieren. In den letzten zehn Jahren konzentrierte sich die Krebstherapie primär auf Tumorzellen.
Mittlerweile zeigt sich jedoch, dass Tumorprogression und Metastasierung keine zellautonomen Prozesse sind, sondern durch multiple Interaktionen mit der Tumor-Mikroumgebung (unter anderem Blutgefäße, Immunzellen, aber auch Thrombozyten) beeinflusst wird. Dieses Milieu stimuliert Tumorwachstum und die Invasion ins gesunde Gewebe, verhindert die Immunerkennung und fördert das Überleben der Tumorzellen im Blutkreislauf, bis sie in entfernten Organen austreten und Metastasen bilden. Gegenwärtig wird angenommen, dass zelluläre und molekulare Komponenten der Tumormikroumgebung eine Barriere bilden, die gegen bestimmte Antikrebsmittel schützt und die Entwicklung von Resistenz gegen therapeutische Ansätze begünstigen kann.
Thrombozyten sind kleine kernlose Zellfragmente, die aus Megakaryozyten im Knochenmark stammen. Über ihre zentrale Rolle in der Hämostase hinaus deutet eine Reihe von Daten darauf hin, dass Thrombozyten diverse Schritte der Krebsentstehung modulieren können. Es wird vermutet, dass Thrombozyten die Tumorangiogenese und das Tumorwachstum unterstützen, und außerdem Tumorzellen vor der Beseitigung durch das Immunsystem schützen. Darüber hinaus erleichtern Thrombozyten die Rekrutierung zirkulierender Tumorzellen an die Gefäßwand und fördern deren Extravasation, wodurch Tumormetastasen unterstützt werden. Darüber hinaus hat eine Meta-Analyse von klinischen Studien gezeigt, dass Aspirin, ein Thrombozyten-Hemmer, die Inzidenz und Ausbreitung von soliden Tumoren reduzieren kann. Obwohl diese experimentellen und klinischen Beweise darauf hinweisen, dass Thrombozyten an der Tumorentwicklung und Metastasierung beteiligt sind, wurden die zugrundeliegenden molekularen Mechanismen noch nicht aufgeklärt.
Unsere Forschungsgruppe konzentriert sich auf die Rolle der Thrombozyten während der Krebsentwicklung. Hierfür verwenden wir Mausmodelle von verschiedenen menschlichen Krebsarten (wie Dickdarm-, Brust-, Melanom-, Lungen- und Leberzellkarzinom) in Kombination mit pharmakologischen Thrombozyten-Hemmern und genetisch veränderten Mäusen. Neben In-vivo-Studien verwenden wir auch modernste Mikroskopietechniken und verschiedene Zellkultursysteme, die es ermöglichen, das Zusammenspiel von Thrombozyten, Tumorzellen, Immunzellen oder Endothelzellen zu untersuchen. Die Perspektive unserer Studie besteht nicht nur darin, unser Wissen über grundlegende Mechanismen von Thrombozyten bei Tumorprogression und Metastasierung zu erweitern, sondern auch neue Krebstherapien vorzuschlagen.


