Gefährliche Thrombozyten besser beherrschen
Thrombozyten helfen bei der Wundheilung im menschlichen Körper. Aber sie können auch wahre Killer sein. Würzburger Forscher haben an ihnen Ansatzpunkte für neue Medikamente entdeckt.
Prof. Nieswandt im Gespräch mit seiner Arbeitsgruppe
Thrombozyten, auch Blutplättchen genannt, sind kleine Zellfragmente im Blut. Wird ein Blutgefäß verletzt, heften sie sich an die betroffene Stelle, lagern sich aneinander und bilden Gerinnsel. So verschließen sie die Wunde und unterstützen die Wiederherstellung des Gewebes.
Vom Helfer zum Killer
„Thrombozyten können lebensrettend sein – aber auch wahre Killer!“, so Prof. Dr. Bernhard Nieswandt. „Denn Thromben, also Blutgerinnsel, sind auch verantwortlich für Gefäßverschlüsse und die daraus resultierende Mangelversorgung von Organen.“ Diese Gerinnsel entstehen häufig an durch Arteriosklerose vorgeschädigten Gefäßwänden. Dort lagern sich Fett, Cholesterin und andere Substanzen ab und bilden Plaques: Die Gefäße werden enger und starrer, wodurch Risse entstehen können.
Dabei wird Kollagen freigesetzt, das normalerweise nicht im Blut vorkommt. Thrombozyten erkennen das Kollagen als Signal, dass eine Verletzung vorliegt, haften sich an die beschädigte Stelle und bilden Blutgerinnsel – die nicht nur den Riss, sondern im schlimmsten Fall das gesamte Gefäß verschließen. „Die Folgen sind Herzinfarkte, Schlaganfälle und auch Lungenembolien. Unzählige Todesfälle gehen somit auf das Konto der Thrombozyten“, so der Leiter des Lehrstuhls für Experimentelle Biomedizin I am Universitätsklinikum Würzburg (UKW) und Forschungsgruppenleiter am Rudolf-Virchow-Zentrum (RVZ) der Universität Würzburg.
Doch Blutplättchen haben noch eine weitere ungünstige Eigenschaft: Sie können auch für Entzündungsprozesse im Körper verantwortlich sein, die bislang dem Immunsystem zugeschrieben wurden. Für diese Kombination aus Gerinnungs- und Entzündungsprozessen prägte Prof. Nieswandt den heute weltweit genutzten Begriff der „Thrombo-Inflammation“ – und gibt ein Beispiel dafür: Ein Patient erleidet einen Schlaganfall durch ein Blutgerinnsel. Das durch das Gerinnsel verengte Gefäß im Gehirn wird mit Medikamenten oder einem Katheter eröffnet. Aber statt sich zu erholen, entwickeln nun zahlreiche Patienten – ebenfalls ausgelöst durch Thrombozyten – Entzündungsreaktionen, die zu schweren Organschäden führen können.

Prof. Dr. Nieswandt im Labor

Prof. Dr. Bernhard Nieswandt
Blockieren ohne Blutungsneigung
Eine Hauptrolle bei den schädlichen Gerinnungs- und Entzündungseffekten spielt ein Rezeptor namens „GPVI“, der sich auf den Blutplättchen befindet. Daher haben Prof. Nieswandt und seine Arbeitsgruppe diesen speziellen Rezeptor untersucht und nach Möglichkeiten geforscht, ihn mithilfe von Antikörper-Bestandteilen zu blockieren.
Die Forschungen haben nicht nur viel grundlegendes Wissen rund um Gerinnungs- und Entzündungsprozesse von Thrombozyten geschaffen, sondern auch zur Entwicklung mehrerer Medikamente geführt, die sich momentan weltweit in fortgeschrittenen Erprobungsphasen befinden.
„Ein entscheidender Unterschied zu anderen medikamentösen antithrombotischen Therapien ist, dass die Blockade des GPVI-Rezeptors nicht zu erhöhter Blutungsneigung der Patienten führt“, erläutert der Experte den besonderen Vorteil der neuartigen Wirkstoffe.
Für die Pionierarbeiten in der Erforschung von Blutplättchen-Eigenschaften wurde Prof. Nieswandt mit einer besonderen Auszeichnung gewürdigt: Im April dieses Jahres erhielt er den mit 2,5 Millionen Euro dotierten „Advanced Grant des European Research Councils“ (ERC) aus dem EU-Programm „Horizon Europe“. Er gehört zu den prestigeträchtigsten wissenschaftlichen Auszeichnungen der EU-Forschungsförderung und ist etablierten Spitzenforscherinnen und -forschern vorbehalten.
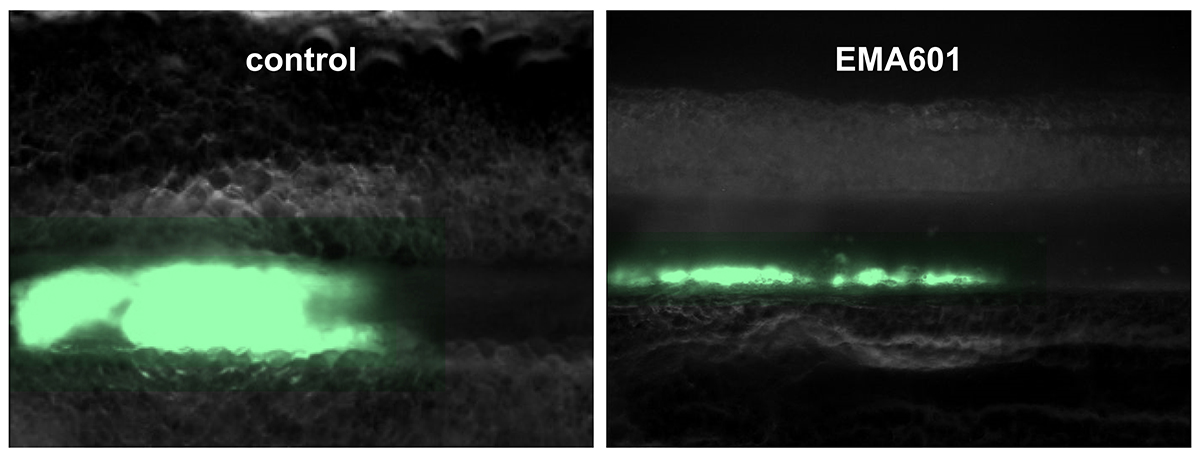
Links: Bei einer unbehandelten Maus blockiert ein Gerinnsel (grün) die Arterie. Rechts: Bei einer behandelten Maus verschließen die Blutplättchen die Wunde, ohne das Gefäß zu verstopfen.